熱力學第一定律基本內容是,熱可以轉變為功,功也可以轉變為熱;消耗一定的功必產生一定的熱,一定的熱消失時,也必產生一定的功。熱力學第一定律是能量守恒原理的一種表達方式。熱力學第二定律,又稱“熵增定律”,表明了在自然過程中,一個孤立系統的總混亂度(即“熵”)不會減小。
熱力學第一定律和第二定律是科學界公認的宇宙普遍規律。能量守恒定律是說,能量可以由一種形式變為另一種形式,但其總量既不能增加也不會減少,是恒定的。二十世紀初愛因斯坦發現能量和質量可以互變后,此定律改為能質守恒定律。這個定律應用到熱力學上,就是熱力學第一定律。
熱力學第二定律是描述熱量的傳遞方向的:分子有規則運動的機械能可以完全轉化為分子無規則運動的熱能;熱能卻不能完全轉化為機械能。此定律的一種常用的表達方式是,每一個自發的物理或化學過程總是向著熵(entropy)增高的方向發展。熵是一種不能轉化為功的熱能。
而熵的改變量等于熱量的改變量除以絕對溫度,高、低溫度各自集中時,熵值很低;溫度均勻擴散時,熵值增高。物體有秩序時,熵值低;物體無序時,熵值便增高。現在整個宇宙正在由有序趨于無序,由有規則趨于無規則,宇宙間熵的總量在增加。
以上就是熱力學第一定律和第二定律的內容 熱力學第一定律和第二定律的內容是什么的內容,下面小編又整理了網友對熱力學第一定律和第二定律的內容 熱力學第一定律和第二定律的內容是什么相關的問題解答,希望可以幫到你。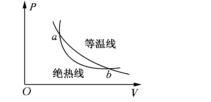
什么是熱力學第二定律?
您好,我是心理學研究僧,很高興回答您的問題,需要了解更多心理學知識,可以點下關注。 一滴可溶于水的墨水滴在水里,墨水會迅速均勻散開。一熱一冷的兩個鐵塊。 滴。
熱力學第二定律的首先提出的是誰?
熱力學第二定律首先提出的是魯道夫·克勞修斯。 1862年被魯道夫·克勞修斯描寫熱力學第二定律。 簡單地說,熱力學第二定律認為封閉系統的熵將會隨著時間的增加。
陳大什么為熱力學第一第二定律規律?
立式管鍋爐。陳大燮是我國熱力工程學界先驅,對熱力學第一、第二定律,蒸汽及內燃周程,蒸汽機原理等方面的研究與教學做出卓越貢獻。抗戰時期,他在重慶設計了一。
熱力學第一定律和熱力學第二定律是相互矛盾的嗎?為什么?
熱力學第一定律是解釋能量的來源與去處,內能通過熱傳遞與做功達到變化。第二定律是指傳遞是有方向性的,總是往宇宙這個大熱力系統熵增的方向進行能量轉換。前。
熱力學第一定律和第二定律地位?
第一定律是能量守恒熱力系內物質的能量可以傳遞,其形式可以轉換,在轉換和傳遞過程中各種形式能源的總量保持不變.第二定律不可能把熱從低溫物體傳到高溫物體而。
熱力學第二定律的兩種表述是什么?微觀統計意義是什么?
熱力學第二定律有兩種基本表述,第一種是(1)克勞休斯表述:不可能把熱量從低溫物體傳向高溫物體而不引起其它變化;第二種是(2)開爾文表述:不可能制成一種循。
高三熱力學第二定律公式?
熱力學第二定律的數學表達式:ds≥δQ/T,又稱克勞修斯不等式。由克勞修斯不等式知,將體系熵變量的大小與過程熱溫熵值進行比較就可以判斷過場可逆與否。 對于絕。
熱力學第二定律實驗原理?
熱力學第二定律(英文:second law of thermodynamics)是熱力學的四條基本定律之一,表述熱力學過程的不可逆性——孤立系統自發地朝著熱力學平衡方向──最大熵。
熱力學第二定律為什么會有兩種完全不同的表述?
題主出此題目,小編微微一笑——題主根本不懂熱力學第二定律!請題主翻翻熱力學教科書,課后習題或者思考題里一定有一道題:請證明熱力學第二定律的兩個描述是等。